リチウムは、軽くて反応性の高い、原子番号3番のアルカリ金属
リチウムの純金属は、水に浮くほど比重が小さくて、しかし、直接、むき出しの金属類に触れると、熱を持って反応します。
そのため、危険性も高いので、単体ではなくて、合金にして使用されます。

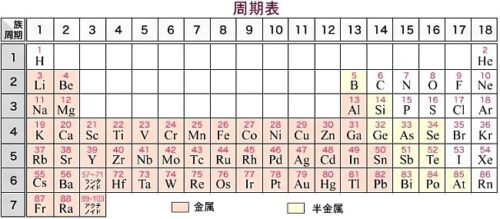
周期表の左端の、1族の、リチウム(Li)、ナトリウム(Na)、カリウム(K)、ルビジウム(Rb)、 セシウム(Cs)、フランシウム(Fr)がアルカリ金属です。
アルカリ金属類は、常温で水を分解して水素を発生し、強塩基の水酸化物をつくる、反応性が高い元素で、アルカリ金属全ては、単体では危険な元素です。
リチウム 元素記号 Li 英語名はLithium
英語名がLithiumで、ここではリチウムと表記することにします。
原子番号3のリチウムは、スマホなどのリチウム電池 という名前は誰もが知っているでしょう。
リチウム電池のなかでもっともよく用いられているのは 二酸化マンガンリチウム電池(CR・FR)や リチウムイオン電池(Li-ion)です。
「リチウム電池」はマンガン電池の10倍以上の電気容量があるので、タフですし電圧低下も少なくて使いやすいのが特徴です。
ところが、劣化して爆発したという危険なことをニュースでも耳にしますから、使用しなくなったリチウム電池は、きめられたとおりに廃棄しなくてはなりません。
リチウム電池は非常に危険なものという認識をして、劣化や取り扱い時の破損には特に注意が必要です。
リチウムはビッグバンで生まれたが生成量は少なかった?
リチウム元素は原子番号3で、ビックバンの際に生まれたものとされていますが、軽くて生成しやすい H(水素)→He(ヘリウム)と、原子番号の順で生まれてきたので、当然、宇宙に存在するリチウムの量もおおむね原子番号の順になっていると予想されるのですが、原子番号順にはなっていません。
宇宙に存在する量は H(水素)→He(ヘリウム)→O(酸素)→C(炭素)→Ne(ネオン)→N(窒素)と続いていて、水素とヘリウムで99.8%ですので、上の周期表にある多くの元素は極端に少ないのです。
さらにリチウムが予想以上に少ないことについて、「宇宙リチウム問題」として現在でも研究対象になっており、(いろいろな仮説はありますが)この理由は、核融合反応の進みやすさのためなどと説明されています。
リチウムの地球の地殻にある順位では25番目の量です。
1位 酸素(47%)、2位 ケイ素(29%)、3位 アルミニウム(8%)、4位 鉄(6%)、5位 カルシウム(4%)、6位 ナトリウム(2%)、7位 カリウム(2%)、8位 マグネシウム(2%)と、以上だけで約98%ですので、リチウムを含めて、有用な金属元素は非常に少ないということがわかります。
リチウム は 金属で軽くて酸化しやすい
金属とは、上の周期表での金属元素とその合金のことで、光沢(金属光沢)があり、展性・延性を有し、電気・熱をよく伝える性質があるものを「金属」といいます。
このリチウムも金属に分類されており、大きな特徴は、金属中で最も軽い金属です。リチウム0.53 →マグネシウム1.74 →ベリリウム1.85 →アルミニウム2.70 と続きますが、水の比重は1.0ですので、(純金属の状態で見ることはありませんが)リチウムは水に浮きます。
しかし、リチウム単体では非常に酸化しやすいので、空気に触れさせないように保管するのですが、リチウムは軽すぎて水やガソリンに入れて保存しようとしても浮いてしまって保存できないために、その表面にワセリンなどの油脂を塗って酸化しないようにして保存されています。
(参考)金属Naも空気に触れると発熱します。比重は0.98で、これは灯油に入れて保管されます。灯油の比重は0.8前後ですので、金属Naは沈むので、空気に触れないようにこの保管法でOKです。
リチウムは、酸化によって発熱しますので単体で使う場合は注意しないといけませんし、もちろん、手で触れても危険です。
このためにそれを防ぐ方法として「合金にして」使用して、酸化や発熱をさけるという使い方をされています。
リチウムの主な用途は 電池 耐水性グリス 触媒 花火の赤色 などです。
リチウム電池は1次電池(使い捨て)と2次電池(充電電池)がある
リチウムを使う、最も一般的な1次電池(コイン型などの充電できない使い捨てのもの)では、電圧が3Vの「二酸化マンガンリチウム電池」があります。CR系と呼ばれるものです。
このCRの「C」が二酸化マンガンリチウム電池を表し、「R」は円形という意味で、CR2032の2032は直径20mmで、厚さが3.2mmを表しています。
CR1216であれば、直径12mmで厚さが1.6mmの丸い二酸化マンガンリチウム電池になります。
余談ですが、LR44などの「L」はアルカリ電池(1.5V)、SR41などの「S」は酸化銀電池(1.55V)です。
1次電池のリチウム電池は充電すると危険ですし、電圧や容量の違うものを一緒に使うのも危険です。飲み込み事故も起きていますから、十分に注意が必要です。
充電して使うリチウムイオン電池(2次電池)にもいろいろな種類があり、種類によって電圧も2.7~4.2Vも違いますし、電気容量もまちまちで互換性はありません。 充電器や使用機器は専用のものを使うようにしましょう。
また、使われている電解液が漏れたり、リチウムの酸化が原因で、爆発事故や火災事故が起きています。
充電電圧には非常に敏感ですので、専用の充電機を使います。過電圧充電や、あらっぽく扱って、外装を傷つけることなどは非常に危険です。
適正な充電をしていても、充電中は電池が熱くなるので、できるだけ、安全な場所で見える状態にしておいて、手で触れない熱さになるなどの異常を感じたら、使用を中止して、適切に廃棄処分するようにします。
グリス・触媒など
自動車用グリスの3割に、耐水性が高く、融点が200℃を超える用途には、ステアリン酸リチウムグリスが使用されています。
また、強化ガラスの原料や、陶磁器の釉薬、合成ゴムイソプレンの触媒などに、リチウムと炭素との有機化合物の炭酸リチウムが使われています。
炭酸リチウムは、リチウムイオン電池の+極に使う、コバルト酸リチウムの原料です。
リチウムの単体では危険性が高いのですが、このような化合物とすることで、危険性が軽減されるので、様々な用途に用いられています。
リチウム塩は躁病の薬
特殊な例としては、炭酸リチウムなどのリチウム塩は、躁病の治療薬として使用されます。
もちろん、リチウムは金属ですから、過剰に摂取すると、肝臓障害をおこす可能性がある毒物です。
サプリメントとして販売されているものもありますが、お医者さんの処方によらなければなりません。
リチウムの炎色反応は赤色

引用ncsm.city.nagoya.jp
ガスバーナーで燃やすと、このように、金属固有の色が出ます。
これを炎色反応といいますが、リチウムの塩類はストロンチウムとともに花火の赤色の発色剤として利用されます。
リチウムの産地とパワーストーンのクンツァイト
リチウムの産地で有名なのはチリのアタカマ塩湖、ボリビアのウユニ塩湖やリンコン塩原などで世界の8割が産出されています。


アタカマ塩湖(上)とウユニ塩湖(下)(いずれもインターネットの記事から)
アタカマ塩湖の塩の中には0.15%のリチウムが含まれていて、このアタカマ湖は(ウユニ塩湖もそうですが)、かつては海であり、アンデス山脈が隆起してできた時に、水が干上がって塩湖になったと考えられています。
つまり、リチウムは海水に含まれているのですが、現在の海水の構成成分を見ると、ナトリウムNaが約32%なのに対してリチウムは0.0004%程度ですので、普通の海水から直接採取するにはコストがかかりすぎるので、現在のリチウムの採取は、塩湖またはペタル石、リチア(リシア)雲母(紅雲母)、リチア(リシア)輝石などの鉱石から採取されています。
ペタル石やリチア輝石はブラジルなどの赤道近くの産出が多いようで、リチア輝石はパワーストーンで名高い「クンツァイト」として非常にきれいな宝石になる鉱石です。
リチウムの語源はギリシャ語のlithos(石)からきているとされています。
1817年にペタル石から発見されており、鉱石や鉱泉に多く含まれることから、何か薬効がありそうな感じもしますが、調べてみますと人間の身体にはあまりよいという内容の記事は見つからず、むしろ有害であるという内容のほうが多いようです。
*****
次の記事 → アルミニウム Al
(来歴)R5年9月に見直し R7.10月に確認


